Zawartość
- etapy
- Część 1 Zrozumienie struktury układu okresowego pierwiastków
- Część 2 Badanie pierwiastków chemicznych
- Część 3 Wykorzystanie masy atomowej do znalezienia liczby neutronów
W chemii układ okresowy pierwiastków jest bardzo ładnym kolorowym obrazem z dużą ilością liter i cyfr, ale idź i zrozum coś! Jest to jednak niezbędne dla każdego, kto chce studiować chemię. Na kompletnej tabeli będziesz w stanie odczytać wiele informacji, które pozwolą ci również wykonać obliczenia (takie jak liczba neutronów w danym jądrze) i rozwiązać wiele problemów chemicznych.
etapy
Część 1 Zrozumienie struktury układu okresowego pierwiastków
-

Umieć czytać układ okresowy. Elementy są sortowane w porządku rosnącym liczb atomowych, od prawej do lewej i od góry do dołu. Liczba atomowa powyżej symbolu jest w rzeczywistości liczbą protonów zawierających atom rozpatrywanego pierwiastka. A ponieważ protony mają masę, masa atomowa pierwiastków rośnie w tym samym kierunku: cięższe atomy (uran) znajdują się na dole, a lżejsze (hel) na górze.- Jeśli masa atomowa rośnie od góry do dołu i od lewej do prawej, dzieje się tak, ponieważ ta ostatnia jest sumą mas protonów i neutronów zawartych w jądrach atomów. Wraz ze wzrostem liczby protonów w macierzy rosną również masy atomowe.
- Z punktu widzenia masy elektrony są uważane za pomijalne wielkości w porównaniu z jądrami.
-

Zauważ, że każdy element ma jeszcze jeden proton niż poprzedni element. Dlatego liczba atomowa rośnie od lewej do prawej i od góry do dołu. Wiersze są kontynuowane w dolnym rzędzie po lewej stronie. Zauważysz także przerwy w pierwszych trzech rzędach.- Pierwszy rząd zawiera tylko dwa pierwiastki, wodór po lewej o liczbie atomowej 1, a hel po prawej o liczbie atomowej 2. Są one odległe, ponieważ należą do różnych grup.
-

Znajdź grupy (lub rodziny) elementów. Wszystkie elementy tej samej grupy znajdują się w tej samej kolumnie, tj. 18 grupach. Każdą kolumnę często można rozpoznać po jednym kolorze. Bycie w tej samej grupie oznacza posiadanie podobnych właściwości fizycznych i chemicznych. Jeśli znasz zachowanie elementu podczas reakcji, będziesz w stanie odgadnąć zachowanie mniej powszechnego elementu tej samej grupy. Wszystkie elementy z tej samej rodziny mają tę samą liczbę elektronów na ostatniej warstwie elektronowej.- Wszystkie pierwiastki należą koniecznie do rodziny chemicznej. W szczególnym przypadku wodór nie należy do żadnej serii: działa tak samo jak alkaliczny jak halogen.
- Większość tabel pokazuje liczbę rodzin (od 1 do 18). Liczby te są oznaczone cyframi rzymskimi (I) lub arabskimi (1), ze szczegółami rodziny lub bez (A = rodzina główna lub B = rodzina drugorzędna).
- Kiedy czytasz kolumnę tabeli, poruszasz się w jej obrębie grupa.
-

Zrozum, dlaczego puste miejsca na obrazie. Pierwiastki są klasyfikowane poziomo według liczby atomowej, ale także pionowo zgodnie z ich strukturą elektronową: elementy kolumny mają te same właściwości chemiczne. Z tych dwóch kryteriów wynika, że tabela przedstawia luki. Wreszcie, bardziej niż liczba atomowa, to struktura atomów najlepiej tłumaczy te wolne przestrzenie.- Tylko z elementu 21 pojawiają się metale przejściowe (skand, tytan ...), które wypełniają luki poprzednich linii.
- Pierwiastki 57 do 102 (lantan, cer ...) należą do grupy metali ziem rzadkich i są reprezentowane przez mały kwadrat w tabeli, który jest wyszczególniony w małym stole na dole głównego stołu.
-

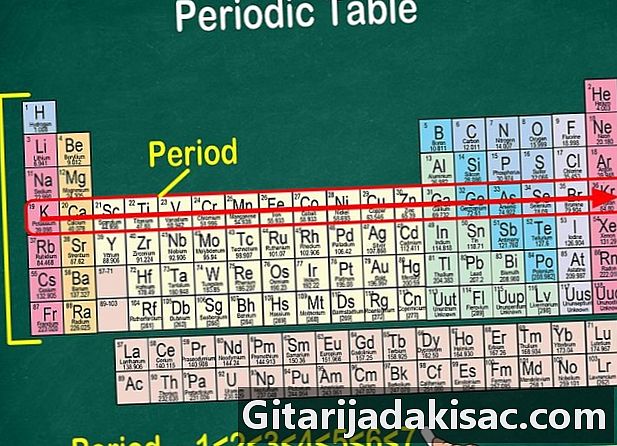
Znajdź okresy. Wszystkie elementy tej samej linii należą do okresu: wszystkie mają taką samą liczbę warstw elektronicznych. Numeracja okresu odpowiada liczbie warstw. PotasK) należy do okresu 4 z powodu tych czterech warstw elektronicznych. W tej chwili żaden znany element nie ma więcej niż 7 warstw elektronicznych.- Aby spojrzeć tylko na ekstremalne okresy, elementy okresu 1 mają tylko jedną warstwę elektronów i te z okresu 7, 7.
- Okresy są najczęściej wskazywane po lewej stronie tabeli, ale tak naprawdę nie ma ustalonej reguły.
- Kiedy czytasz wiersz, poruszasz się w obrębie jednego okres.
-
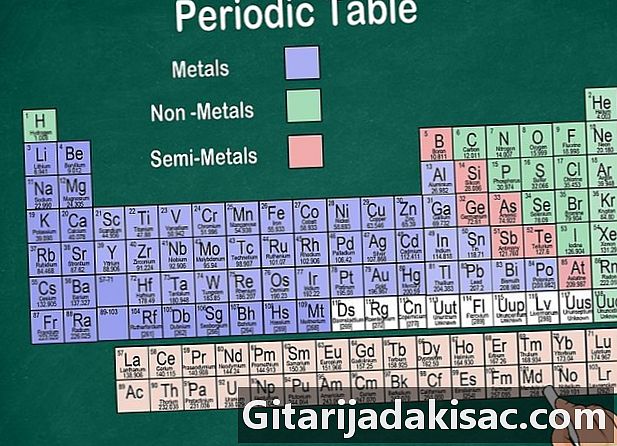
Rozróżnij rodziny elementów. Istnieją zatem między innymi metale, niemetale i między nimi metale przejściowe. Do zmaterializowania tych grup zastosowano kolory. Aby uprościć, powiedzmy, że istnieją trzy główne grupy pierwiastków: metale (cztery podgrupy) po lewej stronie tabeli, niemetale (pięć podgrup) po prawej stronie, a pomiędzy nimi metale przejście- W tej tabeli wodór, z podanych wyżej powodów (pojedynczy proton i pojedynczy neutron), zajmuje specjalne miejsce i ma swój własny kolor: jest niesklasyfikowalny, ale często umieszczany jest w lewym górnym rogu.
- Metale to te elementy, które mają metaliczny połysk, są stałe w temperaturze pokojowej, przewodzą ciepło i elektryczność oraz są plastyczne i ciągliwe.
- Elementy niemetaliczne są uważane za elementy matowe, które nie przewodzą ciepła ani elektryczności i nie są plastyczne. Pierwiastkami tymi są często gazy w temperaturze pokojowej, ale także pewne pierwiastki, które w ekstremalnych temperaturach są ciekłe lub stałe.
- Metale przejściowe mają zarówno właściwości metali, jak i niemetali.
Część 2 Badanie pierwiastków chemicznych
-
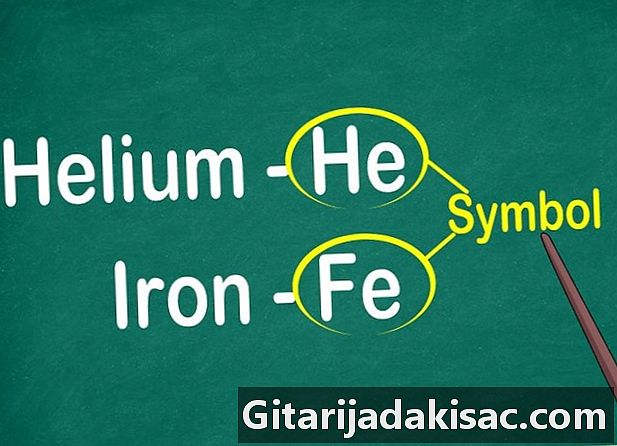
Zauważ, że symbole mają tylko jedną lub dwie litery. Ta informacja pojawia się najwyraźniej na środku każdego kwadratu. Symbole są uniwersalne, aby wszyscy naukowcy mogli się komunikować. Użycie tych symboli jest niezbędne w chemii, szczególnie jeśli chodzi o pisanie równań równowagi z eksperymentów.- Z biegiem czasu powstały symbole i odkrycia. Najczęściej są to pierwsze lub pierwsze dwie litery nazwy elementu. Tak więc symbolem wodoru jest H, podczas gdy hel jest onżelazo Fe... Druga litera często występuje, aby uniknąć pomyłek z innymi elementami (F, Fe, fr dla fluoru, żelaza, frantu).
-

Opcjonalnie zlokalizuj nazwę elementu. W niektórych bardzo kompletnych tabelach nazwa elementu (w języku kraju rozpowszechniania) jest wskazana w kwadracie. Więc pod symbolem C można wydrukować jego imię: węgielpod Sn : cyna (z łaciny Sswójnnum ).- Niektóre tabele okresowe nie zawierają nazw elementów, a jedynie symbole.
-

Znajdź liczbę atomową pierwiastka. Często umieszczane na górze kwadratu, nie ma żadnych zasad dotyczących jego lokalizacji. Jest zawsze dobrze ułożona i często pogrubiona, ponieważ jest to niezbędna informacja. Obecnie istnieje 118 elementów niejawnych.- Liczba atomowa jest zawsze liczbą całkowitą, nie mylić z innymi liczbami kwadratu, czasami dziesiętnymi.
-

Dowiedz się, jaka jest liczba atomowa. Jest to liczba protonów zawartych w danym atomie. W przeciwieństwie do elektronów, które mogą migrować z jednego atomu na drugi, atom nie może stracić ani zyskać protonów, z wyjątkiem fizyki jądrowej, ale to już inna historia!- Ta liczba atomowa umożliwia również obliczenie liczby elektronów i neutronów atomu.
-

Wiedz, że każdy pierwiastek chemiczny ma tyle elektronów, ile protonów. Jest to prawdą, o ile atom nie jest zjonizowany. Protony mają ładunek dodatni, podczas gdy elektrony mają ten sam ładunek ujemny, przy czym oba są zrównoważone w spoczynkowych atomach, ale może się zdarzyć, że podczas reakcji chemicznej atom straci jeden lub więcej elektronów i W takim przypadku otrzymuje się jony dodatnie lub ujemne.- Jony przenoszą ładunek elektryczny. Jeśli jon ma więcej protonów niż elektronów, jest to kation (ładunek dodatni) i dodaje się jeden lub więcej znaków indeksu górnego. Jeśli ma więcej elektronów niż protonów, jest anionem (ładunek ujemny) i jeden lub więcej znaków dodaje się - poprzez odsłonięcie.
- Tylko jony niosą wzmiankę o ładunku, a nie elementy stabilne.
Część 3 Wykorzystanie masy atomowej do znalezienia liczby neutronów
-

Znajdź masę atomową. Masa atomowa jest wpisana na dole kwadratu elementu, pod symbolem. Masa atomowa to masa wszystkich pierwiastków tworzących jądro danego atomu, które zawiera protony i neutrony. Dotyczy to atomów w spoczynku. Jednak do obliczenia tej masy atomowej zdecydowano, że należy przyjąć średnią wszystkich mas atomowych tego pierwiastka w spoczynku, ale także mas wszystkich jego jonów.- Ponieważ te masy są średnimi, masy atomowe są często liczbami dziesiętnymi.
- Po tym, co właśnie powiedziano, logiczne byłoby, aby masy atomowe rosły od lewej do prawej strony obrazu i od góry do dołu, ale nie zawsze jest to regułą.
- Określ względną masę atomową badanego pierwiastka. Uzyskuje się to przez zaokrąglenie masy atomowej do najbliższej liczby całkowitej. Wynika to z faktu, że masa atomowa jest średnią wszystkich mas atomowych różnych form tego pierwiastka, w tym jonów (w rzeczywistości jest to jeszcze bardziej skomplikowane).
- Zatem masa atomowa węgla wynosi 12,011, która jest na ogół zaokrąglana do 12. Podobnie, masa atomowa żelaza wynosi 55,847, zaokrąglona do 56.
-

Oblicz liczbę neutronów. W tym celu konieczne jest usunięcie liczby protonów ze względnej masy atomowej. Względną masę atomową można zsumować do sumy protonów i neutronów atomu, dzięki czemu znając liczbę protonów danego atomu, można z tą względną masą atomową łatwo wydedukować liczbę neutrony!- Użyj następującego wzoru: liczba neutronów = względna masa atomowa - liczba protonów.
- Zatem węgiel ma względną masę atomową 12 i ma 6 protonów. Robiąc 12 - 6 = 6, wywnioskujesz, że rdzeń węglowy zawiera 6 neutronów.
- Żelazo ma względną masę atomową 56 i ma 26 protonów. Robiąc 56 - 26 = 30, wywnioskujesz, że rdzeń węglowy zawiera 30 neutronów.
- Izotopy pierwiastków różnią się od siebie inną liczbą neutronów, przy czym wszystkie protony i elektrony są identyczne. Czyniąc to, wszystkie izotopy mają różne masy atomowe.